阿昔替尼(英利达)与派姆单抗联用一线治疗晚期肾癌。一项临床试验研究了此项联用的安全性和有效性。临床试验结果显示此项联用具有统计学上的临床意义,包括总生存期、客观缓解率、无进展生存期都有延长。
阿昔替尼(英利达)和派姆单抗联用
KEYNOTE-426 (NCT02853331) 研究了阿昔替尼(英利达)联合派姆单抗的疗效,这是一项随机、多中心、开放标签试验,在 861 名未接受晚期肾细胞癌患者全身治疗的患者中进行。无论 PD-L1 肿瘤表达状态如何,患者均被纳入。在过去 2 年内患有需要全身免疫抑制的活动性自身免疫性疾病的患者不符合条件。随机化按国际转移性 RCC 数据库联盟 (IMDC) 风险类别(有利、中等、差)和地理区域(北美、西欧、“世界其他地区”)进行分组。
患者被随机分配 (1:1) 到以下治疗组之一:
阿昔替尼(英利达)5 mg 口服,每天两次,每 3 周一次静脉注射派姆单抗200 mg,持续 24 个月。患者耐受阿昔替尼(英利达)5 mg 每天 2 次共 2 个连续周期(6 周)可增加至 7 mg 和然后随后至 10 mg 每天 2 次。阿昔替尼(英利达)可以中断或减至 3 mg 每天两次和随后至 2 mg 每天两次以控制不良反应。
舒尼替尼 50 mg 口服,每天一次,持续 4 周,然后停药 2 周。
阿昔替尼(英利达)联合派姆单抗的治疗一直持续到 RECIST v1.1 定义的疾病进展或出现不可接受的毒性。如果患者临床稳定并被研究者认为获得临床益处,则允许阿昔替尼(英利达)联合派姆单抗的给药超过 RECIST 定义的疾病进展。肿瘤状态评估在基线时进行,在第 12 周随机化后进行,之后每 6 周一次,直至第 54 周,此后每 12 周一次。
研究人群特征为:中位年龄 62 岁(范围:26 至 90 岁);38% 65 岁或以上;73% 男性;79% 白人和 16% 亚裔;20% 和 80% 的患者基线 KPS 分别为 70 至 80 和 90 至 100;按 IMDC 风险类别划分的患者分布为 31% 有利、56% 中等和 13% 差。
主要疗效结果指标是根据 RECIST v1.1 由 BICR 评估的总生存期和无进展生存期。其他疗效结果指标包括由 BICR 评估的客观缓解率。与舒尼替尼相比,在随机接受阿昔替尼(英利达)联合派姆单抗治疗的患者中,首次预先指定的中期分析显示总生存期有统计学意义的显著改善。该试验还证明了无进展生存期和客观缓解率在统计学上的显着改善。
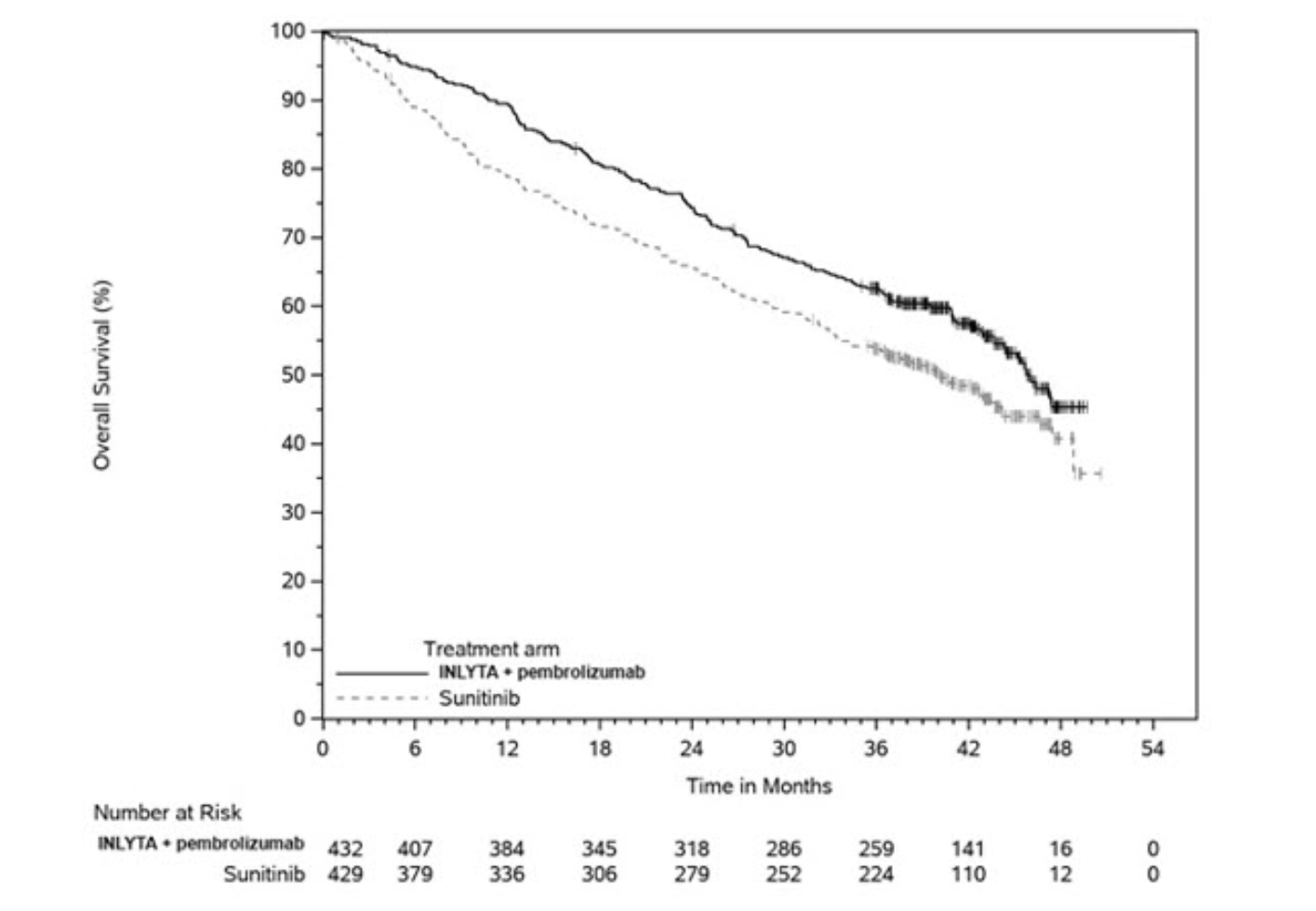
当根据预先指定的最终分析的计划死亡人数观察到 418 人死亡时,进行了更新的总生存率分析。
KEYNOTE-426 中总生存期的 Kaplan-Meier 曲线
总结: 阿昔替尼(英利达)联合派姆单抗一线治疗晚期肾癌的疗效和安全性在临床试验中已经得到证实。患者的总生存期、无进展生存期和客观缓解率都得到了延长。